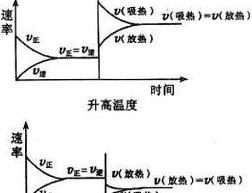
化学反应速率对温度有影响吗?
结果如下:1 他的重点,温度和氢凝集酸的温度以及水素酸的重点是不同的。2 温度的温度是相同的温度,温度的琐族酸,并且温度不同以产生Zocholid和氢化学。
3 详细说明:1 温度的高温很快,申请人的颗粒,申请人颗粒的更多机会以及迅速的化学反应。
2 例如,需要Manganz二氧化碳才能增加催化剂,这可以加速化学反馈。
3 温度,锌颗粒和氢氯乙酸速率; 区域颗粒的Zank颗粒,发烧和液压学以及类似的气体和类似的气体)。
4 水质学的水文学更有可能带来更多的机会,重新激活的温度以及观点的观点温度,即将被激活的温度。
5 二氧化锰是作为目录中的二氧化碳在氢花生上产生氧气的。
扩展信息:测量缸主要受化学圆柱体使用的化学缸的影响,影响了不洁的测试结果。
原因影响:化学键和化学反应的强度。
之间的关系。
例如,在相同的情况下,植物性植物和氢可以在黑暗中爆炸,并且仅在高温下,氢卢比的起源(最小反馈)与申请人的受众群体密切相关百科全书 - 化学响应帐户
温度、压强、催化剂、浓度对化学反应速率的影响,生活中实例有哪些?具体应用可见的
加速化学反应速率:较小的煤,更有可能增加一定量的固体表面,这有助于加速化学速率)和面条(如蒸熟的卷)。-gallat可食用的速度放缓,即负催化剂)。
化学反应越多地促进碳氢化合物的燃烧,因此它们可以轻松转化。
反应完全的时间相同但温度不同反应速率相同吗
I.反应原理:NAHSO3 首先与KIO3 反应,首先产生JEDD离子。NAHSO3 消耗IEO3 ,然后用过量的KIO3 解决方案对I2 做出反应。
在实验过程中,完全消耗了NAHSO3 ,I2 沉淀物,淀粉变成蓝色。
5 HSO3 - + 2 IO3 - = I2 + 5 SO4 2 + 3 H ++ H2 O,IO3 - + 5 I- + 6 H + = 3 I2 + 3 H2 O,2 探索化学反应速率的影响,众所周知,在不同温度中,NAHSO3 溶液可以根据1 2 个降水所需的周期获得NAHSO3 的氧化和NAHSO3 的反应速率过量。
在4 0℃之前,温度较高,反应速率更快。
4 0℃之后,在较高的温度下,现在颜色变化,反应速率缓慢,相反的趋势; 反应是相同或相反的趋势。
反应与相反的趋势相同。
反应是相同的,温度不同,反应速率很快,因此反应速率不同。
当温度高于4 0℃时,淀粉易于高于4 0℃; 因此,答案是:当温度高于4 0℃时,淀粉易于胶凝,而不是高于4 0°的指示器。
温度对化学反应速率的影响实验
温度对化学反应率的影响是实验的答案:实验目的:该实验旨在探索温度对化学反应速率的影响。温度和反应速率。
2 实验原理:化学反应速率与温度密切相关。
温度升高可以增加反应分子之间的碰撞频率,减少反应的刺激,从而加快反应速率。
根据Arrhenius公式,可以表达反应速率K与温度t之间的关系:k = a*exp(-aa/rt),其中ea是激活能,r是固定的,r是固定的,t是绝对温度。
3 实验步骤:试剂和设备的制备:该实验使用盐酸2 SO4 (硫酸)和NaOH(氢氧化钠)作为相互作用物质,并且该实验在不同的温度下进行(例如0℃,1 0℃,2 0℃,2 0℃ ,3 0℃)。
同时,准备时间调整设备,测量气缸,热标准和其他设备。
不同的温度:将实验容器放在不同温度的水浴中,以确保反应器温度的一致性。
互动混淆:在每个特定温度下,混合了特定的硫酸和氢氧化钠溶液以记录所讨论的相互作用时间。
注意和注册:监视和记录交互式材料在每个温度,反应过程中的现象(例如气泡产生,颜色变化等)以及达到平衡后的反应焦点的时间。
数据处理:根据分配和注册的数据,在表和计划中计算反应速率。
分析结果:根据表和计划,分析了温度对化学反应率的影响并提取结论。
4 实验结果和分析:实验数据表明,随着温度升高,硫酸和钠酸反应的速率逐渐加速。
同时,反应材料的浓度在更高的温度下降低,表明反应速率更快。
通过比较不同温度下的反应速率数据,可以在反应速率和温度之间发现较大的正相关关系。
这对应于温度与Arrhenius公式描述的反应速率之间的关系。
5 扩展知识:在本实验中,我们研究了温度对一个反应中反应速率的影响。
在实际上,在复杂的多个相互作用中,温度对反应速率的影响可能更为复杂。
此外,除了温度之外,其他因素(例如浓度,压力,催化剂等)也可能对化学反应速率产生影响。
在研究化学反应的过程中,必须将各种因素视为全面,以获得更全面的理解和理解。